Es la promesa de la medicina con células madre: algún día pronto, las clínicas reconstruirán corazones, riñones, páncreas o sangre enfermos o rotos mediante el crecimiento y la reprogramación de células humanas, y luego las agregarán nuevamente a los cuerpos de los pacientes de los que provienen.
Después de dos décadas de investigación en células madre humanas, los investigadores han aprendido cómo crear versiones que parecen ser razonablemente funcionales de varios tipos de células, primero usando trucos genéticos para volver a las células a un estado no comprometido y luego moldearlas en el tipo de célula necesaria – digamos, una célula productora de insulina o un tipo particular de célula nerviosa. Y muchos ensayos clínicos tempranos de la medicina con células madre han mostrado resultados realmente prometedores.
Pero aplicar tales técnicas en masa simplemente no será práctico, porque los largos procesos para extraer y preparar las propias células de un individuo no aumentarán, dicen algunos científicos.
Por un lado, «las células de todos se comportarán de manera un poco diferente», dice Lonnie Shea, una ingeniera biomédica de la Universidad de Michigan, Ann Arbor. Y luego está el resultado final. «Es más que demasiado caro», dice Douglas Melton, cofundador del Harvard Stem Cell Institute, una red de más de 1,000 científicos afiliados a Harvard.
En cambio, cada vez más, los laboratorios de todo el mundo buscan diseñar terapias celulares disponibles utilizando células donantes universales que están genéticamente alteradas para evitar las respuestas de muchos brazos del sistema inmune contra tejidos extraños. Los científicos quieren crear un conjunto de tales células adaptadas para reparaciones de tejidos específicos: células musculares universales, células universales de la piel o células beta pancreáticas productoras de insulina universales.
«El gran sueño es una célula que sería como una píldora, que podría entrar en cualquier paciente», dice Melton, quien pidió un impulso global para hacer realidad esta visión en una reunión de células madre en Los Ángeles en junio.
Esta tendencia en la medicina regenerativa es paralela a los eventos en la medicina del cáncer. Los tratamientos personalizados que modifican genéticamente las células T de pacientes con ciertos cánceres de sangre a menudo son efectivos, pero tales terapias cuestan cientos de miles de dólares por paciente y la fabricación puede tardar años en ponerse en funcionamiento. Los investigadores de cáncer de todo el mundo ahora están trabajando para crear versiones estándar.
Todo es parte de un esfuerzo más amplio para llevar el poder rápidamente avanzado de la ingeniería genética más profundamente a la medicina regenerativa, dice la hematóloga pediátrica Leslie Kean de la Facultad de Medicina de Harvard, directora del Centro de trasplante de células madre en el Boston Children’s Hospital. «Esto ya no es solo ciencia ficción».
Nuestros cuerpos normalmente rechazan rápidamente cualquier célula que no sea la nuestra. Si bien esa respuesta a menudo puede ser anulada por medicamentos diseñados para suprimir el sistema inmune, estos medicamentos conllevan riesgos y efectos secundarios significativos. Por lo tanto, el objetivo es que las células donantes universales sean «hipoinmunogénicas», capaces de contener las muchas líneas de defensa del sistema inmune sin requerir inmunosupresión.
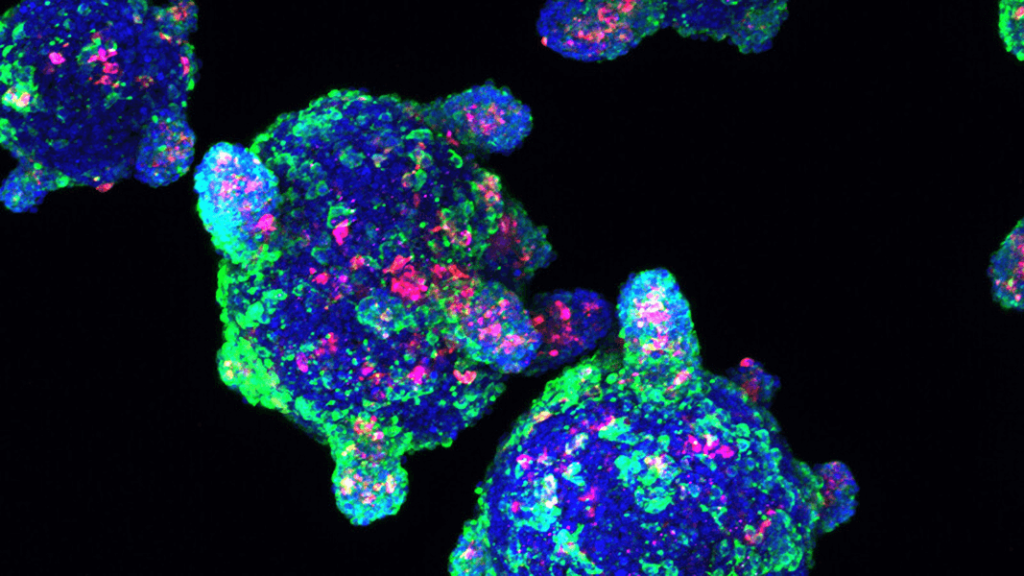
En un desarrollo, los científicos de la Universidad de California en San Francisco y sus colegas informaron en Nature Biotechnology en febrero que habían creado células hipoinmunogénicas de ratón y humano mediante un proceso de varios pasos. Los ingredientes iniciales fueron células iPS (células madre pluripotentes inducidas). Estas son células adultas diseñadas para perder sus identidades celulares específicas para que puedan volver a convertirse en muchos tipos de células diferentes, una condición conocida como pluripotencia. Al manipular algunos genes en estas células iPS, los investigadores podrían producir células cardíacas, células musculares y células endoteliales (que recubren el interior de los vasos sanguíneos). Todos mostraron un comportamiento «sigiloso» a las dos ramas principales del sistema inmunitario, adaptativo e innato, cuando se trasplantaron a ratones.
Para lograr esto, el laboratorio hizo dos cosas. Primero, eliminó varias moléculas del sistema de antígeno leucocitario humano (HLA), componentes del sistema inmunitario adaptativo. Las proteínas de este sistema normalmente cubren la superficie de las células y envían señales de «otredad» a las células T si no coinciden con las del cuerpo.
«Si quitas eso, las células T no pueden reconocer una célula como extraña, y ya no ves la activación de las células T», dice Sonja Schrepfer, autora principal del estudio y directora del Laboratorio de Inmunobiología de Trasplantes y Células Madre de UCSF y una fundación científico de la empresa de nueva creación con sede en Seattle Sana Biotechnology.
Fuente: Knowable Magazine
Eric Bender